硫酸广泛应用于化学加工的化学介质,因它对材料的腐蚀性很强,适宜的结构材料一直是材料生产和设备制造部门关注的焦点。硫酸对金属材料腐蚀的电化学本质,随其浓度的变化而发生较大的变动。就对材料腐蚀而言,25%浓度的H2SO4是还原性酸,随其浓度增加,酸的氧化性也随之增加,但仍以还原性为主,当其浓度大于85%时,它的腐蚀特性就完全变成氧化性酸溶液。
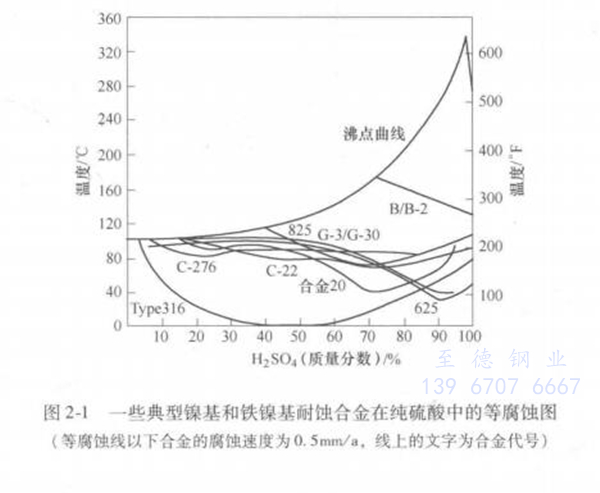
应用实践表明,质量分数小于85%的稀硫酸溶液对金属材料的腐蚀相当严重,其中以50% ~60%最为严苛。在纯硫酸水溶液中,普通含钼不锈钢(316不锈钢) 在浓度小于5%的溶液中可使用到沸腾温度,在40% ~60%浓度的硫酸中在室温已不具备工程可用的耐蚀性,一些高钼含铜的超级奥氏体不锈钢,在最严苛的腐蚀性的硫酸中仅可在60℃以下使用。因此,在高温稀硫酸中最适宜的耐蚀结构材料只能在镍基合金和铁镍基耐蚀合金中寻找。在试剂级硫酸中,一些典型的镍基和铁镍基耐蚀合金的等腐蚀图如图2-1所示。显然,在低浓度纯硫酸中,Ni-Cr-Mo 镍基耐蚀合金和Ni-Cr-Mo-Fe, Ni-Cr-Mo-Fe-Cu铁镍基耐蚀合金较低钼的316型奥氏体不锈钢具有更加优秀的耐蚀性,其使用温度接近酸的沸腾温度。在中等浓度硫酸中,这些合金也仅能在中温使用,大约在100℃以下才具有适用的耐蚀性,仅有镍钼合金可在更高温度的所有浓度的硫酸中具有可用的耐蚀性。然而在含氧化性杂质的酸中,镍钼合金将遭到严重的腐蚀。在1990年面世的高铬、钼含铜的合金31和合金33。在硫酸中呈现出优异的耐蚀性,可与高铬、钼的镍基合金相媲美,见图2-2。
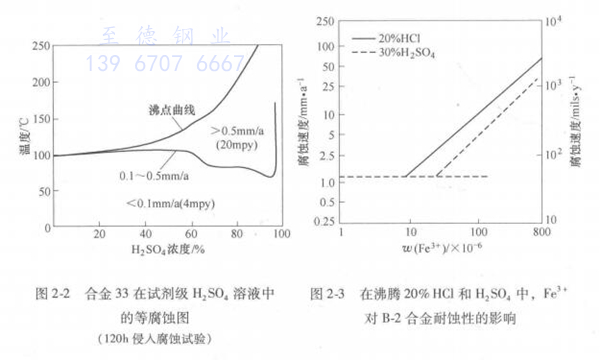
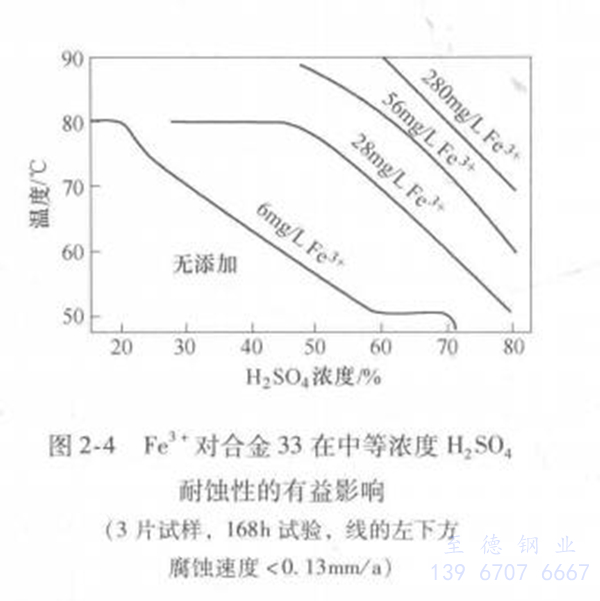
在硫酸中氧化性杂质的存在,对不含铬的镍钼合金的耐蚀性不利,而对含铬的镍铬钼合金的耐蚀性将带来有益的影响,分别见图2-3和图2-4。对于后者是氧化性杂质,除Fe3+外,还有Cu2+和氧,促进合金耐蚀性钝化膜的形成所致。
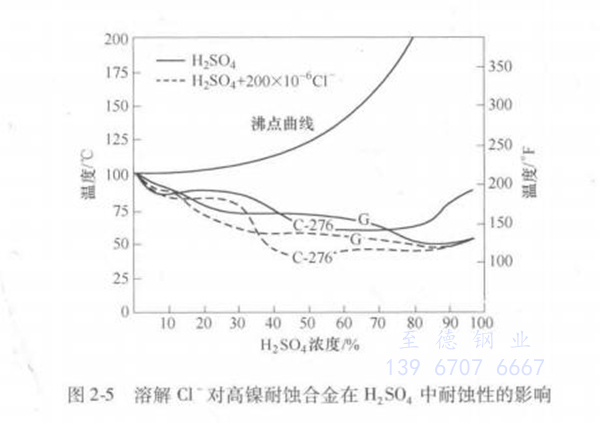
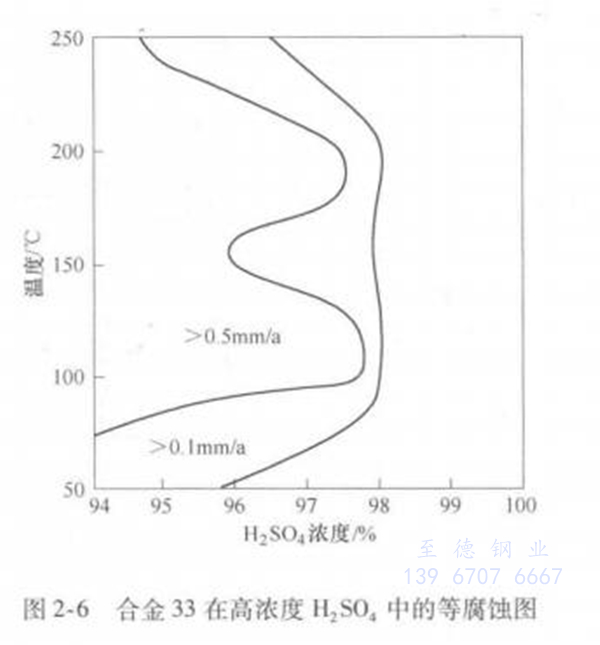
硫酸中的Cl-1将加速合金的腐蚀,其影响程度视合金而定,见图2-5。 高浓度硫酸对金属的腐蚀是属于强氧化性介质,高镍耐蚀合金的耐蚀性强烈受合金中的铬含量所制约,含33%铬的合金33表现出优异的耐蚀性,见图2-6。工厂试验表明,它在硫酸生产中的高浓度H2SO4 (98%)中具有可利用性。这个合金的优势在于它不存在使用高硅奥氏体不锈钢和超级铁素体不锈钢的各种技术障碍,如高硅不锈钢的焊接脆性和超级铁素体不锈钢的截面尺寸限制。



